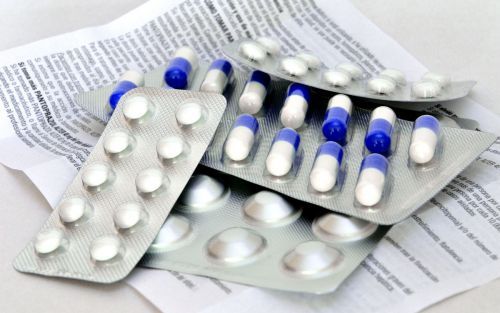
Medicamentos contra la presión arterial que contienen el ingrediente farmacéutico activo Valsartan elaborado por el fabricante Zhejiang Huahai Pharmaceuticals Co. Ltd, China. Fue después de que la Agencia Europea de Medicamentos alertara que se detectó en el proceso de elaboración de dicho ingrediente una impureza: N-nitrosodimethylamine (NDMA), una sustancia potencialmente cancerígena.
Los medicamentos que contienen valsartán se usan para tratar a los pacientes con presión arterial alta para ayudar a prevenir ataques cardíacos y accidentes cerebrovasculares. El retiro preventivo de lotes afecta en la Argentina a siete laboratorios (Richmond, Dr. Lazar y Cia, Temis Lostaló, Baliarda, Elea Phownix, Laboratorio Internacional Argentino y Monte Verde). Para conocer el listado completo de los lotes posiblemente afectados con la impureza en el principio activo se puede ingresar a este link: http://www.anmat.gov.ar/comunicados/retiro_preventivo_Valsartan_ANEXO_18-7-18.pdf
La Anmat sugiere a los pacientes que se encuentren consumiendo alguna de las marcas y lotes detallados, no interrumpir los tratamientos sin consultar a su médico y/o farmacéutico. La suspensión del mismo puede generar consecuencias mayores para su salud y el profesional médico es el indicado para evaluar la alternativa adecuada para cada caso particular y tratamiento.
“Es importante destacar que el principio activo Valsartan no se encuentra cuestionado como hipertensivo y para la insuficiencia cardíaca, sino que el problema se limita a la materia prima proveniente del mencionado fabricante, luego de que se detectara en el proceso de elaboración una impureza potencialmente citotóxica”, aclaró la Anmat en un comunicado.
La EMA fue la primera en anunciar que un fabricante chino del valsartán detectó una impureza en lotes expendidos a distintas empresas a nivel internacional, las cuales se registraron debido a modificaciones en el proceso de elaboración. Hasta el momento 22 países se sumaron al retiro preventivo de medicamentos que contienen el principio activo fabricado por Zhejiang Huahai.
“Todavía es demasiado pronto para proporcionar información sobre el riesgo que la NDMA puede haber causado a los pacientes. EMA ha hecho de este punto de la investigación una prioridad y hará pública la información tan pronto como esté disponible”, informó la Agencia europea.
Ante cualquier duda se puede llamar al Anmat Responde al 0800-333-1234 de lunes a viernes de 8 a 20 hs y sábados, domingos y feriados de 10 a 18 hs.; o bien por correo electrónico a responde@anmat.gov.ar.